Причины и механизм развития гломерулонефрита (этиология и патогенез)
Острый гломерулонефрит
В развитии гломерулонефрита основную роль играет проникновение болезнетворных микроорганизмов, в частности стрептококка, в ткань почки либо воздействие неинфекционных агентов, например, агрессивных химических веществ. Собственная иммунная система организма также повреждает почечную ткань в процессе защиты от вредных факторов. Большое значение имеет и наследственная предрасположенность к данному заболеванию.
Читайте подробнее о симптомах гломерулонефрита.
Основной причиной возникновения гломерулонефрита является стрептококк, который вызывает сначала инфекцию верхних дыхательных путей (ангину, фарингит, скарлатину, обострение хронического тонзиллита) или рожистое воспаление кожи, а при защитных реакциях организма повреждаются почки. Острый гломерулонефрит, возникший таким образом, называют постстрептококковым гломерулонефритом. Другие бактерии и вирусы также могут являться причиной гломерулонефрита, но встречаются они гораздо реже.
Если гломерулонефрит вызван каким-либо видом инфекции, он называется инфекционно-иммунным. Существуют и неинфекционно-иммунные гломерулонефриты. Они могут возникать в результате индивидуальной непереносимости или повышенной чувствительности к лекарственным препаратам, вакцинам, а также любым химическим веществам, пыльце растений, яду насекомых. Алкогольная интоксикация также может стать причиной развития гломерулонефрита. Играет роль и наследственная предрасположенность к развитию гломерулонефрита.
Провоцировать развитие острого постстрептококкового гломерулонефрита могут ОРВИ, переохлаждение, а также носительство стрептококка во рту и/или на коже. Носительство не является болезнью и не заразно для окружающих, однако при снижении иммунитета данный вид бактерий активизируется и вызывает заболевание.
Поскольку ключевым звеном в развитии гломерулонефрита являются иммунные реакции, то для понимания механизма развития заболевания необходимо рассмотреть часть понятий механизмов иммунитета.
Некоторые понятия иммунитета
Иммунитет — это комплекс реакций, направленных на защиту организма от чужеродных агентов (бактерий, вирусов) и веществ, отличающихся от него биологическими (антигенными) свойствами. Сами инфекционные агенты и такие вещества называются антигенами.
Основой иммунитета является лимфатическая система и клетки-лимфоциты, которые в ответ на попадание антигена выделяют особые белки-антитела. Антитела являются специфичными, т. е. на каждый отдельный антиген вырабатывается свой особенный вид антител. Антитела находят антигены и соединяются с ними, образуя комплекс «антиген-антитело» (АГ-АТ), затем происходит уничтожение антигенов.
Ликвидация антигенов может происходить разными путями. Один из них — активация комплемента (с комплиментом для дамы не имеет ничего общего). Система комплемента — это комплекс белков плазмы крови, которые активизируются при определенных условиях, например, при образовании комплексов АГ-АТ, и помогают удалению антигенов.
Активация комплемента связана с местной воспалительной реакцией, которая сопровождается расширением сосудов, увеличением их проницаемости и выходом жидкости из сосудистого русла в межклеточные пространства. Это необходимо для того, чтобы нейтрофилы — особый вид лейкоцитов, — которые непосредственно уничтожают антигены, быстрее попали в место их локализации. Конечный результат этих реакций — разрушение антигенов.
Отложение иммунных комплексов
При остром постстрептококковом гломерулонефрите антигенами являются токсины, которые выделяет данный микроорганизм. При других видах заболевания это могут быть токсины или частички прочих микробов, белки, содержащиеся в лекарственных средствах, компоненты опухолей больного человека и пр. Они циркулируют в крови, а потом заносятся в почку (т. к. вся кровь фильтруется через почки), где откладываются на базальной мембране (клеточной стенке) капилляров клубочков.
Попадание антигенов в организм вызывает выработку антител, которые находят и соединяются с чужеродными агентами, вызывая формирование иммунного комплекса. Сформированные иммунные комплексы вызывают активацию системы комплемента.
Активация комплемента
Комплемент участвует в защите организма от бактерий, вирусов, опухолевых клеток, однако при ряде заболеваний, в том числе при гломерулонефрите, комплемент вызывает развитие воспаления. Одной из реакций при деятельности системы комплемента является формирование комплекса, который разрушает клеточную стенку антигена-мишени. При гломерулонефрите такой мишенью, кроме непосредственно антигенов, становится базальная мембрана капилляров клубочков.
В обычных условиях антигены из комплекса АГ-АТ разрушаются особым видом лейкоцитов. Но при гломерулонефрите комплексы осаждаются на базальной мембране, и лейкоциты не могут до них добраться. Поэтому они выделяют вещества, которые должны разрушить антиген, рядом с комплексом АГ-АТ, а значит, и рядом с базальной мембраной. В итоге базальная мембрана также повреждается от их действия.
Эти же лейкоциты выделяют вещества, способствующие свертыванию крови, активизирующие воспаление и увеличивающие пропускную способность базальной мембраны клубочков. Теперь через базальную мембрану могут проходить крупные молекулы белка, и возникает выделение белка с мочой — протеинурия.
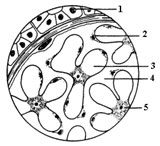
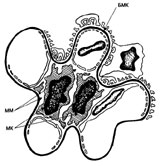
Роль различных клеток в развитии гломерулонефрита
При гломерулонефрите наблюдается выраженное разрастание мезангиальных клеток. Это клетки, которые располагаются между капиллярами клубочка; они синтезируют межклеточное вещество и поддерживают форму клубочков почки. Увеличение количества мезангиальных клеток обусловлено влиянием комплемента, иммунными комплексами, токсинами и веществами, которые выделяются при воспалении.
Процесс разрастания мезангиальных клеток играет большую роль в развитии гломерулонефрита, т. к. сопровождается продукцией веществ, усиливающих воспалительную реакцию. Кроме того, данные клетки вырабатывают вещества, привлекающие к себе лейкоциты и активирующие свертываемость крови.
Рядом с капиллярами клубочков находятся эпителиальные клетки, сходные по строению с клетками нашей кожи. Они также разрастаются под влиянием биологически активных веществ, выделяющихся в очаге воспаления. Эпителиальные клетки продуцируют вещества, стимулирующие свертывание крови. Разрастание эпителия может обусловить тяжелое течение гломерулонефрита.
Активированные тромбоциты тоже выделяют вещества, способствующие развитию воспалительной реакции, а также формируют микротромбы в капиллярах клубочков.
В последние годы определенная роль в механизмах развития гломерулонефрита отводится активации апоптоза. Апоптоз — запрограммированная клеточная смерть — активируется при разрастании мезангиальных клеток и различных видов лейкоцитов в почечной ткани. Предполагается, что активация апоптоза способствует очищению клубочков от избытка воспалительных масс и восстановлению его структуры. Активация апоптоза способствует выздоровлению больного острым гломерулонефритом. Его же депрессия (снижение активности) способствует переходу острого гломерулонефрита в хронический.
Быстропрогрессирующий (подострый, злокачественный) гломерулонефрит
Механизмы развития этого вида гломерулонефрита такие же, как и при остром гломерулонефрите. Неблагоприятным признаком считается развитие некротизирующего артериита (воспаления сосудов почек, сопровождающегося омертвением клеток).
Хронический гломерулонефрит
Хронический гломерулонефрит чаще всего является результатом перенесенного острого гломерулонефрита. Возможно возникновение т. н. первично-хронического гломерулонефрита без предшествующего острого периода. Причины возникновения хронической формы заболевания такие же, как и для острой, но часто причину болезни выявить не удается.
Механизмы развития, в целом, аналогичны таковым при остром гломерулонефрите, т. е. в основе лежит иммунный воспалительный процесс. Но большую роль в прогрессировании заболевания играют и неиммунные механизмы. Это развитие соединительной ткани в почках, увеличение свертываемости крови, повышение артериального и внутриклубочкового давления, нарушения в жировом обмене организма.
Развитие прогрессирующего фиброза в почках
Во всех органах, и в почках в том числе, кроме основной ткани, выполняющей функциональную нагрузку, существует еще и соединительная ткань. Она отвечает за поддержание формы органа, защищает его и участвует в питании. При хроническом воспалении соединительная ткань становится более плотной, а местами напоминает рубец — развивается фиброз.
Участки фиброза неуклонно увеличиваются, чему способствуют разросшиеся мезангиальные клетки. Именно они продуцируют вещества, которые становятся основой соединительной, а затем и рубцовой ткани. Прогрессирующий фиброз является основой хронической почечной недостаточности. На начальных этапах формирования фиброза при адекватном лечении возможно полное восстановление структуры клубочков.
Повышение артериального и внутриклубочкового давления
При хроническом прогрессирующем гломерулонефрите клубочки утрачивают свои функции. Чтобы почки как-то выполняли свою работу, оставшиеся клубочки увеличиваются в размерах и вынуждены работать «за двоих». Теперь через уцелевшие почечные клетки должно проходить гораздо больше жидкости, чем в норме. Повышение функции сохранившихся клубочков всегда сопровождается внутриклубочковым повышением давления, чтобы обеспечить более интенсивную работу.
При повышенном давлении в клубочках резко повышается проницаемость базальной мембраны капилляров, что способствует проникновению в мезангиальный матрикс (вещество, окружающее мезангиоциты) белка, жиров и других компонентов плазмы. Эти компоненты, откладываясь в матриксе, стимулируют рост мезангиоцитов и продукцию веществ, которые приводят к замещению клубочков соединительной тканью (склерозированию).
В результате заболевания активизируется работа гормонов, отвечающих за повышение артериального давления, которое усиливает повышение давления внутри клубочков и нарушение доставки кислорода к почкам. Эти процессы также способствуют склерозированию почек.
Нарушение жирового обмена в организме
При гломерулонефрите повышается уровень холестерина крови, изменяется соотношение различных видов жиров, что ведет к их отложению в почках. Нарушения жирового обмена оказывают токсическое влияние на почки, а при отложении жиров в почечных структурах активируются мезангиоциты, что опять же ведет к разрастанию соединительной ткани.
Увеличение свертываемости крови
Свертывание крови с образованием микротромбов и отложением белка фибрина в капиллярах клубочков является одним из самых важных механизмов прогрессирования хронического гломерулонефрита. Фибриновые отложения стимулируют рост мезангиоцитов, способствуя разрастанию соединительной ткани, снижают кровоснабжение и доставку кислорода к клеткам почек. Увеличению свертываемости крови и отложению фибрина способствует повреждение токсинами и иммунными комплексами внутренней ткани, выстилающей капилляры.
Роль тубулоинтерстициального склероза
Термин «тубулоинтерстициальный склероз» означает, что рубцовая, плотная соединительная ткань разрастается в «тубулах» — канальцах почек и уплотняет интерстициальную ткань — рыхлую соединительную ткань, которая не несет функциональной нагрузки, а поддерживает форму и участвует в питании органа.
Клетки иммунной системы, участвующие в воспалительном процессе, активируют клетки канальцев, которые вырабатывают вещества, повреждающие интерстициальную ткань почек и способствующие развитию там фиброза. Длительное выделение с мочой белка также оказывает токсическое влияние на интерстиций почки.
Читайте о том, как нужно лечить гломерулонефрит.
Все перечисленные механизмы прогрессирования приводят к длительному воспалительному процессу, который течет волнообразно, с периодами усиления и затухания заболевания. Хроническое воспаление приводит в итоге к склерозированию, разрастанию хрящеподобной ткани, запустеванию всё большего числа клубочков и потере ими своей функции, развитию хронической почечной недостаточности.
Задайте свой вопрос доктору.
* - обязательные поля.
|
|